Contexte scientifique :
Le diagnostic précoce et précis des cancers est crucial pour améliorer les résultats pour les patients et optimiser l'utilisation des ressources cliniques. La biopsie est une procédure médicale essentielle dans ce processus, mais la sélection des sites de biopsie demeure une étape critique et complexe, souvent basée sur des critères visuels ou des indications cliniques générales. Le projet de recherche proposé vise à développer un outil d'assistance au choix de biopsie innovant, basé sur la combinaison de la spectrométrie de fluorescence1,2 et de l'apprentissage machine3, pour améliorer la précision diagnostique en oncologie.
Le/la candidat·e retenu·e pour cette thèse travaillera en étroite collaboration avec des experts en spectrométrie de fluorescence, en apprentissage machine et neurochirurgie et en oncologie clinique. Les objectifs spécifiques de la thèse incluront :
1. La collecte et l'analyse de données de spectrométrie de fluorescence à partir de tissus biologiques prélevés lors de biopsies cliniques. En particulier, nous souhaitons utiliser des fluorophores endogènes (ex : NADH, flavine, PPIX, …) afin d’obtenir des informations biologiques encore plus précises que dans nos travaux antérieurs1,2.
2. Le développement et la validation de modèles d'apprentissage machine capables de reconnaître les caractéristiques morphologiques et moléculaires associées à des lésions spécifiques. Dans le détail, nous souhaitons évaluer différents modèles de ‘machine learning’ et de ‘deep learning’ pour l'analyse approfondie et la classification des spectres optiques obtenus à partir des tissus de glioblastomes
3. L'intégration de ces modèles dans un outil informatique convivial qui peut être utilisé par les cliniciens pour guider la sélection des sites de biopsie.
4. L'évaluation de l'efficacité et de la précision de l'outil à l'aide de données cliniques indépendantes et de tests prospectifs au bloc opératoire.
|
|
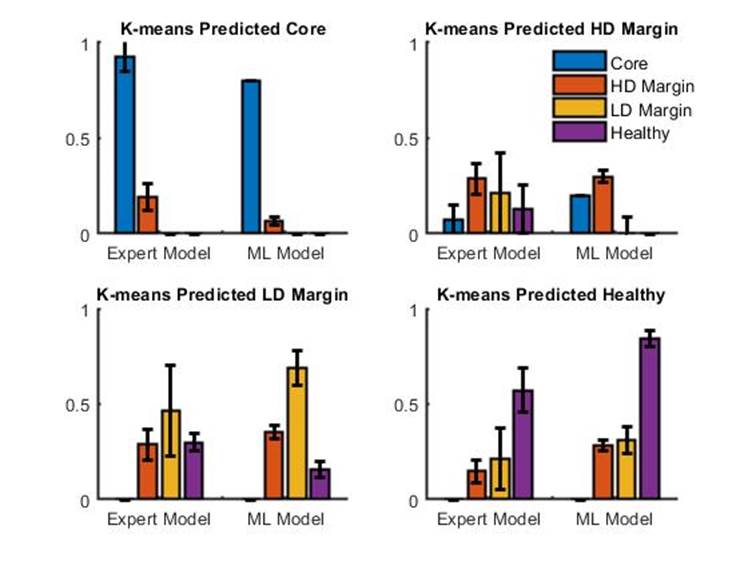
Expériences in vivo pendant une opération | Comparaison “Machine Learning model” vs “Expert model” |
Le/la candidat·e aura l'opportunité de travailler sur un projet de recherche innovant et interdisciplinaire, avec des applications pratiques potentielles importantes pour la pratique clinique. Les résultats de la thèse pourraient contribuer à améliorer la précision diagnostique, à réduire les complications associées aux biopsies inutiles et à optimiser les résultats pour les patients atteints de cancer. Le/la candidat·e acquerra des compétences précieuses en spectrométrie de fluorescence, en apprentissage machine et en oncologie clinique, ainsi qu'une expérience pratique dans la conception, la mise en œuvre et l'évaluation d'outils d'assistance médicale innovants.
Profil du/de la candidat.e :
Le/la candidat·e idéal·e pour cette thèse doit avoir un diplôme de master/ ingénieur avec des compétences en analyse de données, en traitement de données et en machine learning, une appétence pour l’instrumentation. Le/la candidat·e doit avoir de solides compétences en programmation, une capacité à travailler en équipe et une forte motivation pour mener des recherches interdisciplinaires dans le domaine de la santé. Une bonne connaissance de l'anglais écrit et parlé est requise.
Encadrement et financement :
Le/la candidat·e sera encadré·e par une équipe interdisciplinaire composée d'experts en spectrométrie de fluorescence, en apprentissage machine en neurochirurgie et en oncologie clinique. Dans le détail l’encadrement sera assuré par :
Cédric RAY-GARREAU (CREATIS)
Thiebaud Picart (Neurochirurgien aux Hospices Civils de Lyon)
Arhur Gautheron (CREATIS)
Le projet de thèse sera financé par une allocation doctorale de la Graduate School Medical Device5 et s’inscrit dans le cadre du projet Européen EIC Pathfinder Hyperprobe4.
Perspectives :
Les perspectives pour cette thèse incluent l'exploration de nouvelles techniques d'imagerie et de détection, telles que l'imagerie par fluorescence in vivo. En intégrant des données multimodales et en exploitant des approches d'intelligence artificielle plus avancées, il est possible de développer des outils encore plus sophistiqués pour la prise de décision clinique. Le/la candidat·e aura également l'opportunité de poursuivre une carrière académique ou industrielle dans le domaine en pleine expansion de la médecine personnalisée et de la santé numérique.
Contact :
Cédric RAY-GARREAU / cedric.ray[a_remplacer]univ-lyon1.fr / www.creatis.insa-lyon.fr/
Références :
- B. Montcel, L. Mahieu-Williame, X. Armoiry, D. Meyronet, and J. Guyotat, “Two-peaked 5-ALA-induced PpIX fluorescence emission spectrum distinguishes glioblastomas from low-grade gliomas and the infiltrative component of glioblastomas,” Biomedical Optics Express 4, 548 (2013). (https://doi.org/10.1364/BOE.4.000548).
- Gautheron, M. Sdika, M. Hébert, et B. Montcel, “An explicit Estimated Baseline Model for Robust Estimation of Fluorophores using Multiple-Wavelength Excitation Fluorescence Spectroscopy," IEEE Transactions on Biomedical Engineering (2023). (https://doi.org/10.1109/TBME.2023.3299689).
- P. Leclerc, C. Ray, L. Mahieu-Williame et al. “Machine learning-based prediction of glioma margin from 5-ALA induced PpIX fluorescence spectroscopy”. Sci Rep 10, 1462 (2020). (https://doi.org/10.1038/s41598-020-58299-7).
- Le projet HyperProbe reçoit un financement du programme de recherche et d'innovation Horizon Europe de l'Union européenne dans le cadre de l'accord de subvention n° 101071040. (https://hyperprobe.eu/).
- Graduate school for medical devices : https://graduate-plus.fr/en/medical-device-engineering-2/